Transferwege für Protonen beim zellulären Energiestoffwechsel
Struktur und Funktionsweise eines zentralen Biomoleküls der Atmungskette untersucht.
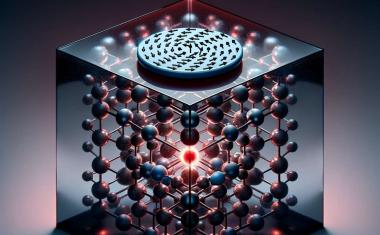
Alle Lebensprozesse erfordern eine ständige Versorgung mit Energie. In der Zelle wird diese Energie hauptsächlich über das chemisch aufgeladene Molekül ATP zur Verfügung gestellt. Erzeugt werden die ATP-Energiepakete unter anderem in speziellen Organellen der Zelle, den Mitochondrien. Über die Atmungskette werden Wasserstoffionen – also Protonen – von einer Seite der inneren Mitochondrien-Membran auf die andere gepumpt, sodass ein chemisches Konzentrationsgefälle und eine elektrische Spannung entstehen. Entlang dieses elektrochemischen Gradienten fließen die Protonen durch eine Art Turbine, die für die Zelle nutzbare Energie in Form von ATP erzeugt.
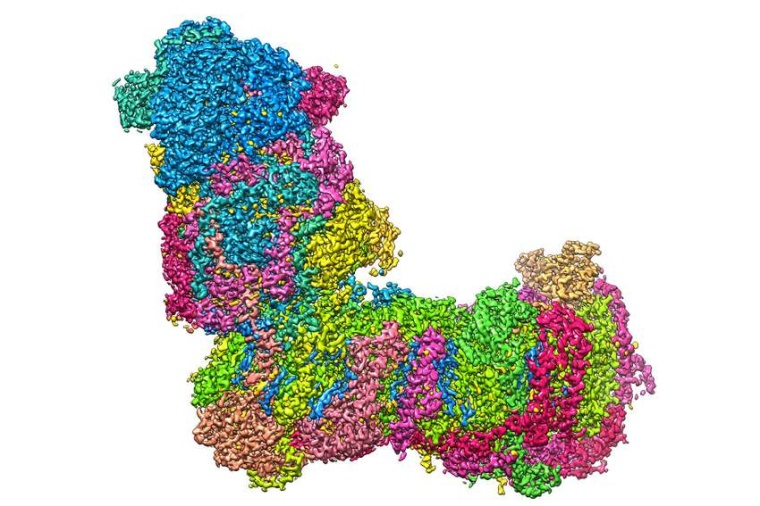
Eine der Protonenpumpen im ersten Schritt des Prozesses ist ein großes, L-förmiges Biomolekül, der mitochondriale Komplex I. Mit seinem waagerechten Arm ist das L in der Membran verankert. Am senkrechten Arm des L bindet er das Elektronenträgermolekül NADH, das aus der Verstoffwechselung beispielsweise von Zucker stammt. Komplex I katalysiert die Übertragung von Elektronen von NADH auf Ubichinon und die in dieser Reaktion freiwerdende Energie wird zum Antrieb der Protonenpumpe genutzt.
Einem Forscherteam der Uni Frankfurt und des MPI für Biophysik in Frankfurt ist es jetzt gelungen, die 3D-Struktur von Komplex I mithilfe des hochauflösenden Bildgebungsverfahren der Kryoelektronenmikroskopie exakt zu vermessen und abzuleiten, auf welchen Wegen die Protonen innerhalb des Komplex I transportiert werden. Hierbei spielen, so konnten die Wissenschaftler zeigen, Wassermoleküle in der Proteinstruktur eine wichtige Rolle.
Die hochaufgelösten Strukturdaten ermöglichten umfangreiche Computersimulationen durch Forscher der Uni Helsinki, die zeigten, wie sich die Pumpe während des Protonentransports wahrscheinlich bewegt. Die Studie gibt neue Einblicke in die Funktionsweise einer molekularen Maschine der biologischen Energieumwandlung. Dieses Wissen kann dazu beitragen, bestimmte mitochondriale Krankheiten besser zu verstehen.
GFU / RK
Weitere Infos
- Originalveröffentlichung
K.Parey et al.: High-resolution structure and dynamics of mitochondrial complex I—Insights into the proton pumping mechanism, Sci Adv. 7, eabj3221 (2021); DOI: 10.1126/sciadv.abj3221 - Structural Bioenergetics, Institut für Biochemie II, Goethe-Universität Frankfurt
- Abt. Strukturbiologie, Max-Planck-Institut für Biophysik, Frankfurt am Main