Wie das Gehirn zu seinen Nährstoffen kommt
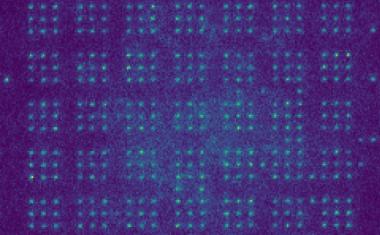
Experimentell vermessene Adernetzwerke zeigen Bedeutung der Selbstorganisation von Kapillar-Netzwerken.
Das Zellgewebe von Tieren und Pflanzen wird von einem komplexen vaskulären Netzwerk, den Blutgefäßen durchzogen. Dieses versorgt die Zellen in dem Gewebe mit Nährstoffen. Tiere können einzelne Kapillaren durch Muskeln weiten, um die Nährstoffversorgung in dem vaskulären Netzwerk anders zu verteilen. Doch wie müssen die Kapillaren geweitet werden, um mehr Nährstoffe in einen bestimmten Bereich des Zellgewebes zu transportieren? Hängt die Änderung der Nährstoffverfügbarkeit für eine Zelle stark von der Position der Zelle im Gewebe ab? Haben vaskuläre Netzwerke einen speziellen Aufbau, der ihnen erlaubt, die Nährstoffzufuhr präzise zu steuern, wenn nur bestimmte Bereiche des Zellgewebes mehr Nährstoffe benötigen? Diesen Fragen gingen Felix Meigel und Karen Alim von der Arbeitsgruppe „Biologische Physik und Morphogenese“ am Max-Planck-Institut für Dynamik und Selbstorganisation (MPIDS) nach.
In einer neuen Arbeit haben die beiden Grundlagenforscher beschrieben, wie viele Nährstoffe in der Mikrovaskulatur entlang einzelner Kapillaren an das Gewebe abgegeben werden. Ihr Ergebnis: Der Aufbau und die Struktur eines Netzwerkes sind zweitrangig, wenn der Transport der Nährstoffe entlang der Kapillaren durch den Blutfluss dominiert wird.
Blut transportiert Sauerstoff, Hormone und Nährstoffe durch vaskuläre Systeme zu den Zellen in einem Gewebe. Die stärkste Nährstoffabgabe erfolgt dabei in Kapillaren, die ein kompliziertes Netzwerk bilden. Falls eine Zelle einen höheren Nährstoffbedarf hat, sendet die Zelle Signalstoffe aus, die kleine Muskeln an den Kapillaren weiten oder verengen. So lässt sich der Blutfluss und somit auch die Versorgung mit Nährstoffen lokal verändern. In Netzwerken jedoch können kleine lokale Änderungen sehr große Auswirkungen hervorrufen. Um genau vorherzusagen, wie sich der Blutfluss nach einer Kapillarerweiterung ändert, ist es notwendig, die Selbstorganisation der gesamten Netzwerktopologie zu kennen. Dabei tauchen Fragen auf wie: Ist die Kapillarerweiterung ein Problem für Zellen in einem Gewebe? Wie kann garantiert werden, dass zuverlässig mehr Nährstoffe zu den Zellen gelangen, die mehr Nährstoffe benötigen?
Mit einer Kombination aus theoretischen Modellen und Computersimulationen an experimentell vermessenen Adernetzwerken untersuchten Felix Meigel und Karen Alim, wie sich die Nährstoffversorgung ändert, wenn eine einzelne Kapillare geweitet wird. Dabei fanden die Forscher heraus, dass nicht nur der Transport zu einer Ader entscheidend ist, sondern auch inwieweit die Kapillare die Nährstoffe aufnehmen kann. Verändert sich die Blutflussgeschwindigkeit oder der Durchmesser einer Kapillare, ändert sich auch die Menge der Nährstoffe, die in der Kapillare absorbiert und an das umliegende Gewebe abgegeben wird. Dabei gibt es drei Absorptionsmöglichkeiten, zum Beispiel je nachdem, wie schnell das Blut fließt: Entweder absorbiert die Kapillare fast alle durchströmenden Nährstoffe oder es dominiert der Transport per Blutfluss durch die Kapillare oder es findet nur ein langsamer, diffuser Transport in der Kapillare statt.
In mehr als 99 Prozent der Kapillaren dominiert in der Mikrovaskulatur der Transport mit dem Blutfluss, der advektive Transport. Für diese Kapillaren puffert die Absorptionsdynamik die Änderungen der Transportdynamik durch das Weiten der Kapillare ab. Die Nährstoffversorgung wird somit robust verstärkt, unabhängig von der genauen Positionierung der Kapillare im komplexen vaskulären Netzwerk. Darüber hinaus gilt als Daumenregel, dass die Kapillaren, die auf die geweitete Kapillare folgen, ebenfalls eine höhere Nährstoffversorgung erhalten.
„In meiner Arbeitsgruppe arbeiten wir an der Frage, wie sich biologische Transportnetzwerke an veränderte Umwelteinflüsse anpassen. Die Mikrovaskulatur ist ein Paradebeispiel für ein sich anpassendes Transportnetzwerk. Wir wollen verstehen, wie Transport und Versorgung von Gewebe in einem Netzwerk zusammenhängen, das sich selbst verändern kann“, sagt Forschungsgruppenleiterin Karen Alim. „Wenn wir neuronale Aktivitäten diagnostisch vermessen, nutzen wir dafür die funktionelle Magnetresonanztomographie (fMRI). Dabei messen wir aber nicht die neuronale Aktivität selbst, sondern eine Veränderung des Blutflusses. Aber wie man die tatsächliche neuronale Aktivität mit einer beobachteten Veränderung der Durchblutung in Verbindung bringt, ist eine offene Frage. Mit unserem Formalismus geben wir eine Handreichung dafür, wie aus dem Blutfluss auf die Zellversorgung in einem Gewebe geschlossen werden kann. Damit können wir verstehen, wie sich die Zellversorgung ändert, wenn sich der Blutfluss ändert. Dies ist von grundlegender Bedeutung, um letztlich die Frage zu beantworten, wie eine erhöhte neuronale Aktivität mit einer Veränderung der Durchblutung verbunden ist“, sagt Felix Meigel.
Mit der vorliegenden Arbeit gewinnen die Grundlagenforscher ein besseres Verständnis dafür, wie sich unser Gehirn selbst zu jeder Zeit selbst organisiert. Die Erkenntnisse, die die MPIDS-Wissenschaftler hier gewonnen haben, helfen aber auch in ganz anderen Bereich weiter. „In Zukunft können wir beispielsweise Medikation besser verstehen oder auch wie künstliche Gewebe funktional designt werden sollte. Aber auch für die Verbesserung chemischer Reaktoren, die oft aus porösen Medien bestehen, ist unser Formalismus hilfreich.“, sagt Gruppenleiterin Alim.
MPIDS / DE
Weitere Infos
- Originalveröffentlichung
F. J. Meigel et al.: Robust increase in supply by vessel dilation in globally coupled microvasculature, Phys. Rev. Lett. 123, 228103 (2019); DOI: 10.1103/PhysRevLett.123.228103 - Biologische Physik und Morphogenese (K. Alim), Max-Planck-Institut für Dynamik und Selbstorganisation. Göttingen